Σε προειδοποιητική επιστολή με ημερομηνία 5 Μαρτίου, η Υπηρεσία Τροφίμων και Φαρμάκων (FDA) κατέγραψε πέντε περιπτώσεις όπου ασθενείς που λάμβαναν τα φάρμακα υπέστησαν εγκεφαλικό, εξέφρασαν αυτοκτονικές σκέψεις ή πέθαναν – μία από αυτές τις περιπτώσεις αφορούσε αυτοκτονία – χωρίς η εταιρεία να τις αναφέρει σωστά.
Η FDA σημειώνει ότι οι ενέργειες της Novo Nordisk «υποδηλώνουν συστημικές αποτυχίες στην παρακολούθηση, καταγραφή, αξιολόγηση και αναφορά» πιθανών παρενεργειών.
Εκπρόσωποι της εταιρείας δεν έδωσαν συγκεκριμένο αριθμό ασθενών που επηρεάστηκαν όπως αναφέρει η USATODAY, ωστόσο ανάλυση δεδομένων της FDA από το USA TODAY δείχνει μεγάλη αύξηση στις αναφορές παρενεργειών τον Ιούλιο του 2025, λίγους μήνες μετά από σχετικό έλεγχο.
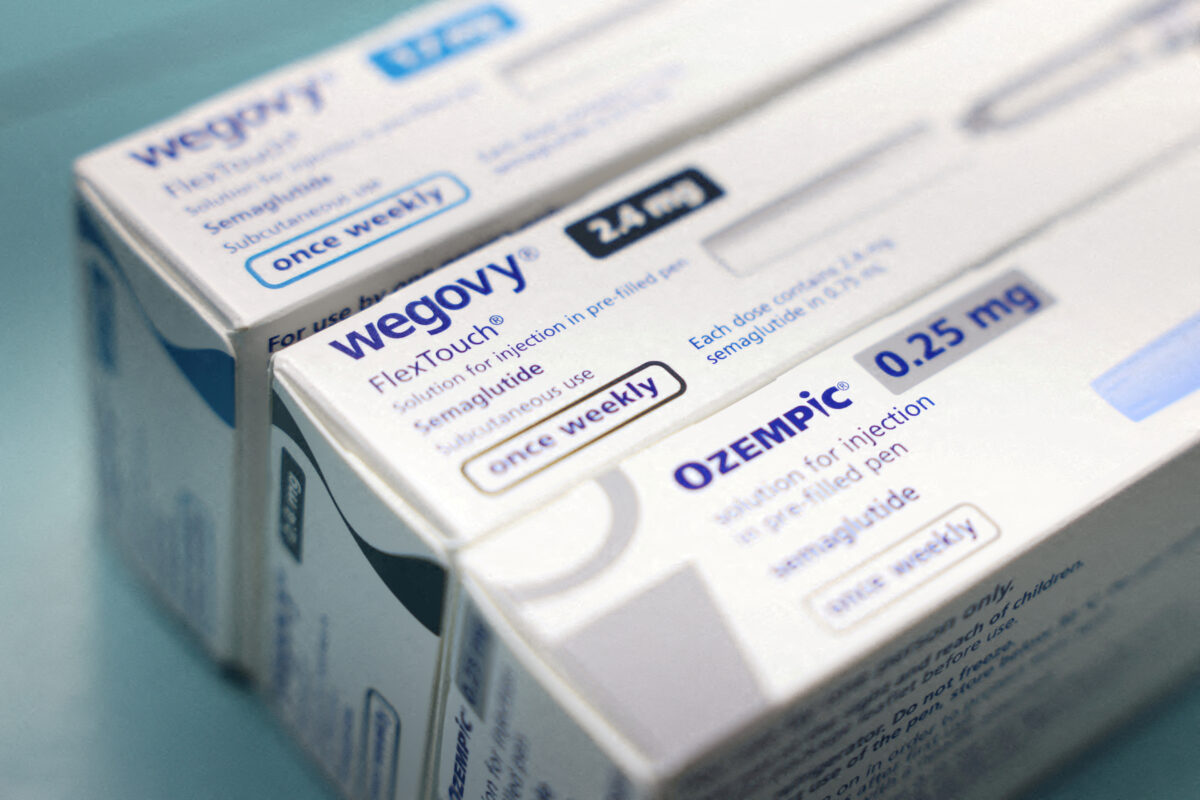
Μόνο σε μία εβδομάδα, η εταιρεία υπέβαλε σχεδόν 11.000 αναφορές παρενεργειών που σχετίζονται με τη σεμαγλουτίδη, τη δραστική ουσία των Ozempic και Wegovy. Από αυτές, περισσότερες από 1.800 χαρακτηρίστηκαν σοβαρές – κατηγορία που περιλαμβάνει θάνατο ή απειλητικές για τη ζωή αντιδράσεις και πρέπει να δηλώνεται εντός 15 ημερών.
Οι υπόλοιπες 9.100 αναφορές αφορούσαν μη σοβαρές παρενέργειες, όπως ναυτία ή εμετό.
Η Novo Nordisk δεν εξήγησε τον χρόνο υποβολής αυτών των στοιχείων, αλλά δήλωσε ότι δεσμεύεται να αντιμετωπίσει τα προβλήματα που εντοπίστηκαν στον έλεγχο της FDA.
Η εκπρόσωπος της εταιρείας, Λιζ Σκρμπκόβα, τόνισε ότι «η ασφάλεια και η αποτελεσματικότητα των φαρμάκων GLP-1 διασφαλίζονται όταν χρησιμοποιούνται σωστά και υπό ιατρική παρακολούθηση».
Διευκρίνισε επίσης ότι οι αναφορές παρενεργειών δεν αποδεικνύουν ότι το φάρμακο προκάλεσε το περιστατικό, αλλά απλώς ότι ο ασθενής το λάμβανε τη στιγμή που συνέβη.
«Η FDA δεν υποστήριξε ότι τα φάρμακα προκάλεσαν αυτά τα συμβάντα, αλλά ότι δεν αναφέρθηκαν σωστά», σημείωσε. «Η χρήση όρων όπως “θάνατος” ή “σοβαρό ανεπιθύμητο συμβάν” είναι συνηθισμένη σε τέτοιες αναφορές».
Χιλιάδες ασθενείς έχουν ήδη καταθέσει αγωγές κατά της εταιρείας, κατηγορώντας τη ότι υποβάθμισε τους κινδύνους των φαρμάκων της. Ο δικηγόρος Τζόναθαν Όρεντ, που εκπροσωπεί πολλούς ενάγοντες, δήλωσε ότι η επιστολή της FDA «υποτιμά σημαντικά το μέγεθος του προβλήματος» και στερεί από γιατρούς και ασθενείς κρίσιμες πληροφορίες.
Η FDA δεν έχει ανακοινώσει κυρώσεις μέχρι στιγμής, ωστόσο τέτοιες επιστολές αποτελούν συνήθως το πρώτο βήμα για τη διαπίστωση παραβάσεων και την απαίτηση συμμόρφωσης.
Πρόκειται για την τρίτη προειδοποιητική επιστολή προς την εταιρεία μέσα σε έξι μήνες, καθώς πρόσφατα εντοπίστηκαν τρίχες ζώων σε φιαλίδια φαρμάκων σε εγκατάσταση στην Ιντιάνα και κρίθηκε παραπλανητικό διαφημιστικό υλικό για τα φάρμακα αδυνατίσματος.
Τι καταλογίζει η FDA
Η νέα επιστολή περιγράφει περιστατικά όπου η εταιρεία δεν διερεύνησε αναφορές παρενεργειών, τις απέρριψε αδικαιολόγητα ή καθυστέρησε να τις αναφέρει.
Η αμερικανική νομοθεσία απαιτεί από τις φαρμακευτικές να αναφέρουν σοβαρές παρενέργειες εντός 15 ημερών, ανεξάρτητα από το αν θεωρείται ότι σχετίζονται άμεσα με το φάρμακο.
Ωστόσο, σύμφωνα με την FDA, η εσωτερική πολιτική της Novo Nordisk επέτρεπε την απόρριψη αναφορών αν οι ασθενείς ή οι γιατροί δεν πίστευαν ότι το φάρμακο ευθυνόταν.
Σε ένα παράδειγμα, ασθενής που υπέστη εγκεφαλικό ενώ λάμβανε λιραγλουτίδη (δραστική ουσία των Victoza και Saxenda) δεν αναφέρθηκε, επειδή ο ίδιος δεν το συνέδεσε με το φάρμακο.
Οι ελεγκτές κατηγορούν επίσης τα τηλεφωνικά κέντρα της εταιρείας ότι απέρριπταν αναφορές λόγω ελλιπών στοιχείων. Σε μία περίπτωση, άνδρας που πέθανε ενώ λάμβανε σεμαγλουτίδη δεν δηλώθηκε ποτέ, παρότι τα στοιχεία του υπήρχαν στα αρχεία.
Αν και η εταιρεία απαιτούσε δύο προσπάθειες για συμπλήρωση στοιχείων, επέτρεπε την απόρριψη αναφορών ασθενών που δεν είχαν δώσει συγκατάθεση για περαιτέρω επικοινωνία – κάτι που, σύμφωνα με την FDA, δεν απαιτείται από τη νομοθεσία.
Η επιστολή αναφέρει επίσης ότι η εταιρεία δεν διερεύνησε περιστατικά κατάθλιψης και αυτοκτονικού ιδεασμού, καθώς και έναν θάνατο ασθενούς που λάμβανε σεμαγλουτίδη.
Παρότι η Novo Nordisk έχει τροποποιήσει τις πολιτικές της μετά τον έλεγχο του 2025, η FDA θεωρεί τα μέτρα ανεπαρκή και εκφράζει σοβαρές ανησυχίες για την ικανότητα της εταιρείας να διασφαλίσει την ασφάλεια των φαρμάκων της.
Χιλιάδες αγωγές από ασθενείς
Περίπου το 12% των ενηλίκων στις ΗΠΑ – πάνω από 31 εκατομμύρια άνθρωποι – χρησιμοποιούν φάρμακα GLP-1.
Αν και πολλοί ασθενείς έχουν δει αποτελέσματα με ήπιες παρενέργειες, αυξάνεται ο αριθμός όσων καταγγέλλουν σοβαρές επιπτώσεις, όπως τύφλωση, νευρολογικές διαταραχές και εντερικά προβλήματα.
Μέχρι τις 16 Μαρτίου, τουλάχιστον 5.000 άτομα έχουν κινηθεί νομικά κατά φαρμακευτικών εταιρειών, συμπεριλαμβανομένης της Novo Nordisk και της Eli Lilly, που παράγει τα Trulicity, Mounjaro και Zepbound.
Οι εταιρείες απορρίπτουν τις κατηγορίες και δηλώνουν ότι θα υπερασπιστούν την ασφάλεια των φαρμάκων τους.
Ο δικηγόρος Όρεντ δήλωσε ότι τα ευρήματα της FDA επιβεβαιώνουν όσα καταγγέλλουν οι ενάγοντες εδώ και χρόνια και χαρακτήρισε την κατάσταση «ανησυχητική», εκφράζοντας φόβους ότι ασθενείς που λαμβάνουν άλλα φάρμακα της εταιρείας μπορεί να μην μάθουν ποτέ τις επιπτώσεις στην υγεία τους.
Σε ανακοίνωσή της, η Novo Nordisk υποστήριξε ότι η επιστολή της FDA ζητά κυρίως διευκρινίσεις για τη συμμόρφωση με τους κανονισμούς και «δεν καταλήγει σε συμπεράσματα για την ποιότητα ή την ασφάλεια των φαρμάκων».
Ειδήσεις Σήμερα
- Τζέιν Φόντα: Σκληρή επίθεση κατά της Μπάρμπρα Στρέιζαντ – Ο Ρόμπερτ Ρέντφορντ η αφορμή για το beef – «Εγώ έπρεπε να είμαι εκεί» [βίντεο]
- Σεισμός στα Ιωάννινα: Εγκλωβισμένος εργάτης μετά από κατολίσθηση
- Οι δύο εμφανίσεις που τους μπέρδεψαν όλους: Κρις Τζένερ και Λόρεν Σάντσεζ με τα ίδια λουκ στο πάρτι του Vanity Fair
- Ποιος θέλει τι από τον πόλεμο στο Ιράν – Τα κρυφά σχέδια ΗΠΑ, Τεχεράνης και Ισραήλ
- Ο Δημήτρης Ουγγαρέζος σε ένα επικό σχόλιο: «Αν η Σία Κοσιώνη χτυπήσει το χέρι στο τραπέζι, την ακούει όλος ο ΣΚΑΙ»